实际气体除了p-v-T关系在定量上与理想气体状态方程有较大的偏差以外,在一定条件下将发生集态的变化(或称相变),转变成液态或者固态,是实际气体的一个很重要的性质。
图7-6 实际气体p-v-T 关系
图7-6表示在p-v图上的临界点c、饱和液态线、饱和蒸气线以及一组定温线簇。
压力低于临界压力时,通过冷却或加热,工质会凝结或气化。在凝结或气化过程中,物质呈现为蒸气和液体两相平衡共存的混合物。物质处于不同的相且能平衡共存的状态称为饱和状态。一种物质,在一定温度下达到饱和状态时,总是处于确定的压力,这个压力称为对应于该温度的饱和压力,用符号Ps表示;反过来说也是一样,物质在一定压力下达到饱和时总是处于确定的温度,这个温度称为对应于该压力的饱和温度,用符号Ts表示。
液体在气化过程中,由于容积膨胀,增加了内位能和对外作了膨胀功,因此要吸收一定量的热。1kg饱和液体全部转变为饱和蒸气在气化过程中吸收的热量称为气化潜热,用符号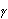 表示。按照热力学第一和第二定律,
表示。按照热力学第一和第二定律,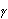 与饱和液及饱和蒸汽的各种状态参数有如下关系
与饱和液及饱和蒸汽的各种状态参数有如下关系
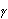 =(u″-u′)+Ps(v″-v′)
=(u″-u′)+Ps(v″-v′)
=h″-h′=T(s″-s′) (8-11)
式中u′、v′、h′及s′分别表示饱和液的比内能、比体积、比焓及比熵;u″、v″、h″及s″分别表示饱和蒸气的比内能、比体积、比焓及比熵;Ps及Ts是气化时的饱和压力及饱和温度。气化潜热的数值与气化时的温度(或压力)有关。
在较低温度下(低于三相点温度Ttp),气体达到饱和时直接转变为固相,这个过程称为固化;固态达到饱和时直接转变为气体,称为升华。液体在定压下冷却,还将达到饱和而转变成固态,这个过程称为凝固;它的逆过程,固体达到饱和而转变为液体叫做熔解。升华和熔解过程的情况和气化过程是相似的:过程中物质呈现为不同的相平衡共存的混合物;它们也都在相对应的饱和压力及饱和温度下发生;升华和熔解过程也要吸收一定量的热量,分别称为升华潜热和熔解潜热,它们也都有如式(8-11)的关系式。但是,升华和熔解过程的上界线(饱和蒸气线及饱和液线)和下界线(饱和固态线)没有发现有交点,也就是说没有发现临界点,这是它们不同于气化过程的地方。
一般习惯用p-T图表示物质的相图,如图8-7所示。在p-v图Oc线表示了气化时饱和压力与温度的函数关系,称为气化线。气化线上方端点c是临界点。曲线OA和OB分别称为升华线和熔解线。气化线、升华线和熔解线统称为饱和曲线,它们相交于一点O。在O点固、液、气三相都处于饱和状态,是物质能够处于固、液、气三相平衡共存的唯一的状态点,称为三相点。每种物质的三相点有确定的温度Ttp和压力Ppt数值。
 收藏此帖
收藏此帖 收藏此帖
收藏此帖