安德留斯(Andrews)作了如下的实验:在一封闭管中装有液态 CO2,将管加热,当温度达 31.1℃ 时,液体和蒸气的界面突然消失。高于此温度时无论加多大的压力,都无法再使气体 CO2 液化。这种现象在其它液体实验中同样也可以观察到。安德留斯把能够以加压方法使气体液化的最高温度,称为"临界温度"(以 Tc 表示);在临界温度下为使气体液化所需施加的最小压力,称为"临界压力"(以 pc 表示);物质在临界温度和临界压力下的摩尔体积,称为"临界摩尔体积"(以 Vc,m 表示),三者总称临界参数(表1-5)。而由临界温度 Tc 和临界压力 pc 决定的状态,称为"临界状态"或"临界点"。
表1-5 一些气体的临界参数
| |
pc(kPa) |
Vc,m(10-3dm3mol-1) |
Tc(K) |
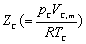 |
He
Ne
Ar
Xe
H2
O2
N2
F2
Cl2
Br2
CO2
H2O
NH3
CH4
C2H4
C2H6
C6H6 |
229.0
2725.6
4863.6
5876.8
1297.0
5076.4
3394.4
5572.9
7710.8
10335.2
7376.4
22088.8
11247.1
4640.7
5116.9
4883.9
4924.4 |
57.8
41.7
73.3
119
65.0
78.0
90.1
-
124
135
94.0
55.3
72.5
99
124
148
260 |
5.21
44.4
150.7
289.8
33.2
154.8
126.3
144
417.2
584
304.2
647.4
405.5
191
283.1 |
0.306
0.308
0.285
0.290
0.305
0.308
0.291
-
0.276
0.287
0.275
0.227
0.242
0.289
0.270
0.285
0.274 |
图1-9为气体液化等温线的示意图。在临界温度 Tc 的等温线以上的区域为气态,在此范围内无论加多大压力都无法使气体液化。低于 Tc(图中的 T1、T2、T3)低压时仍为气态,但在临界温度以下的气体常称为"蒸气",当压力增加至一定值时(例如图中沿 T1 等温线将蒸气压缩至相当于 A1 点),开始有液体的出现。 继续加压,体系压力不变,但随着体积减小,体系中液体比例愈来愈大,至 B1 点时,全部蒸气变为液体。此后加压,体系压力随着增加,而液体的可压缩性远较蒸气为小,体积随压力变化关系变得陡削。在 A1 至 B1 这段范围内,气液两态共存,表示这一阶段的平台线,称为"结线"。由上图可见,随着温度升高,结线变短,达到临界温度时,收缩成为一点。这一现象说明随着温度升高,气、液两态密度差别愈来愈小,在临界点时趋于相等。
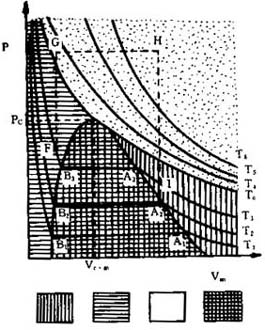
图1-9 实际气体典型液化等温线 |
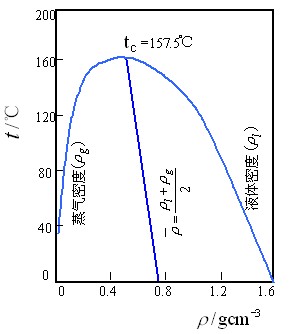
图1-10 SO2 平均密度随温度变化的线性关系 |
由液态转变为气态,并不一定需要经过气液两态共存这一过渡阶段才能实现。如图,欲使液态 F 转变为等温下的气态 I,可以选取沿 T3 等温线减压经气液共存区最后达到 I 态的途径;也可以自 F 态开始,先在恒容条件下加压升温,当达到临界温度 Tc 时,由液变气是连续的,即没有出现两态共存的情况,高于 TC 时进入了气态区,达 G 态后,在恒压下升温由 G 态达 H 态,继之在恒容下降压降温最后达气态 I。这一转变过程是连续性的,说明气、液两态在这种情况下并无明显的区别,对气体和液体概称为"流体"则更为合适。这种现象显示出可以用某些气体状态方程式来描述液体的行为。
临界温度和临界压力比较容易直接测量,临界摩尔体积的测量则较困难,常利用同一温度下液体和蒸气的密度平均值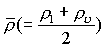 随温度变化成线性关系,间接地用外推法求出,图1-10为应用这一关系以求出 SO2 的临界密度的示意图。
随温度变化成线性关系,间接地用外推法求出,图1-10为应用这一关系以求出 SO2 的临界密度的示意图。
 收藏此帖
收藏此帖 收藏此帖
收藏此帖